Was Sie über Disease Interception wissen müssen
- Titus Kaletta
- 13. Juli 2022
- 7 Min. Lesezeit
Aktualisiert: 19. Juni 2023

Krankheiten zu erkennen, zu behandeln und sogar zu heilen, bevor der Patient Symptome entwickelt, klingt fast zu schön, um wahr zu sein, aber es ist genau das, was die so genannte "Disease Interception" verspricht. Das frühe Abfangen von Krankheiten ist ein neues Forschungsgebiet zur Behandlung von Alzheimer, Krebs und bestimmte andere chronische Erkrankungen. Wir stellen dieses Konzept vor und diskutieren den Einsatz von künstlicher Intelligenz.
Eine der größten Herausforderungen des modernen Gesundheitswesens ist die Früherkennung und Prävention von Krankheiten. Diese Herausforderungen werden durch eine alternde Bevölkerung und eine höhere Lebenserwartung noch vergrößert. Chronisch fortschreitende Krankheiten wie Alzheimer oder Krebs sind schwer zu heilen, sobald die ersten klinischen Symptome auftreten. Eine frühzeitige Erkennung von Alzheimer oder bestimmten Krebsarten vor dem Auftreten von Symptomen und damit eine tatsächliche Vorbeugung wäre der Heilige Gral im Gesundheitswesen: Mit Hilfe von Datenanalyse und künstlicher Intelligenz könnte dies in Zukunft tatsächlich Wirklichkeit werden. Der Ansatz heißt "Disease Interception". Er würde es Ärzten und Krankenhäusern ermöglichen, Patienten so früh wie möglich zu diagnostizieren, ihre Krankheiten zu erkennen und ihr Entstehen vorzubeugen. Patientinnen, könnten sich in vorbeugenden ärztliche Behandlung begeben, bevor die eigentliche Krankheit ausbricht. Was ist die Vision hinter diesem neuen medizinischen Konzept? Ist es wirklich neu? Wir stellen dieses Konzept vor und erörtern die anstehenden Herausforderungen.
Inhalt
Disease Interception - eine spezielle Form der Sekundärprävention
Disease Interception (DI) ist eine neue Strategie zur Prävention von Krankheiten. Im Falle der Alzheimer-Krankheit bedeutet Interception, dass die Krankheit frühzeitig diagnostiziert wird, bevor das Gehirn bereits erheblich geschädigt wurde. Aber was genau ist Disease Interception? Die folgenden vier Kriterien grenzen DI von anderen Präventionsstrategien wie beispielsweise der Krebsvorsorge oder Gentests ab (1):
Der Krankheitsverlauf hat bereits begonnen, ist aber klinisch noch unauffällig,
Aus dem Frühstadium der Krankheit wird sich mit hoher Sicherheit das volle klinisches Bild entwickeln, wenn nicht rechtzeitig eingegriffen wird,
Es gibt nur ein bestimmtes Zeitfenster, um einzugreifen, und
Eine Intervention bzw. Therapie ist verfügbar und individuell angepasst.
So kann zum Beispiel das Prostatakarzinom-Screening mit Hilfe des PSA-Tests dazu beitragen, ein Risiko für den Patienten frühzeitig zu erkennen. Allerdings bedeutet ein erhöhter PSA-Wert nicht gleich, dass sich ein bösartiger Tumor entwickeln wird. Der Patient hat nun zwar die Information, dass er ein Risiko hat, an Prostatakrebs zu erkranken, aber außer einer regelmäßigen Überwachung gibt es heute keine Möglichkeit der Vorbeugung (eine vorbeugende Operation der Prostata würde als Überbehandlung gelten). Diese Art der Prävention unterscheidet sich von der DI, da sie das zweite und vierte Kriterium nicht erfüllt (der PSA-Test ist dennoch ein wertvolles Diagnoseinstrument!). Wir wollen die DI am Beispiel der Alzheimer-Krankheit (AD) erläutern.
Die Rolle von Disease Interception bei Alzheimer
Die Alzheimer-Krankheit (AD) ist ein gutes Beispiel für die Nützlichkeit der DI. Die meisten Alzheimer-Patienten entwickeln die Krankheit im Alter von über 65 Jahren. Die Frühdiagnose erfolgt durch mentale Tests und in zunehmendem Maße durch biomolekulare Marker-Tests für Tau und Beta-Amyloid. Das Problem ist, dass die Alzheimer-Krankheit lange vor dem Auftreten von Symptomen und dem Nachweis dieser Biomarker beginnt. Alzheimer-Patienten bemerken im Frühstadium keine Symptome, ebenso wenig wie Angehörige und Freunde. Doch wenn die Alzheimer-Erkrankung diagnostiziert wird, ist das Gehirn bereits geschädigt - die Krankheit begann schon viele Jahre zuvor.
Ein kürzlich entwickeltes Medikament gegen Alzheimer ist gescheitert, obwohl es vor allem auf Patienten im Frühstadium der Alzheimer-Krankheit abzielte und weil die Schädigung des Gehirns bereits vorhanden war. Das Fortschreiten der Krankheit konnte durch das Medikament nicht aufgehalten werden. Offenbar gibt es ein Zeitfenster zwischen einem gesunden Gehirn und einem erkrankten Gehirn mit klinischen Symptomen, das die Möglichkeit bieten würde, die Krankheit rechtzeitig zu behandeln. Leider ist weder dieses Zeitfenster bekannt (es ist vermutlich unterschiedlich lang, zwischen einigen Jahren und über einem Jahrzehnt, und es kann sich im Alter von 50 Jahren, aber auch in späteren Jahren öffnen), noch ist der genaue Auslöser für Alzheimer bekannt.
Alzheimer vor dem eigentlichen Entstehen zu verhindern bedeutet, Menschen zu identifizieren, die ein hohes Risiko haben, die Krankheit zu entwickeln, sie durch regelmäßige Untersuchungen sorgfältiger zu überwachen und die Krankheit abzufangen (zu behandeln), bevor sie sich entfalten kann. Der Gedanke dahinter ist, dass eine sehr frühe Erkennung der Krankheit wirksamere Behandlungen, mildere Eingriffe oder sogar Heilung ermöglichen könnte.
Künstliche Intelligenz als entscheidendes Instrument für Disease Interception
Forscher suchen schon seit vielen Jahren nach Biomarkern für sehr frühe Krankheitsstadien oder Krankheitsvorstufen. Der Einsatz künstlicher Intelligenz (KI) könnte ein neuer Weg sein, diese Vision wahr werden zu lassen. Jüngste Fortschritte im Bereich des maschinellen Lernens bieten neue Instrumente, die bei der Erforschung von Krankheitsvorstufen helfen können. Ein Forscherteam unter der Leitung von Dr. Anke Diehl, Chief Transformation Officer der Universitätsmedizin Essen, nutzt beispielsweise KI, um das Fortschreiten der Alzheimer-Krankheit bei einer Gruppe von Patienten auf der Grundlage ihrer genetischen Daten vorherzusagen (2). "Um frühe Hinweise auf eine Krankheit zu finden, müssen große Datenmengen, Big Data, gesammelt und analysiert werden. Der Mensch allein kann dies nicht leisten; künstliche Intelligenz ist erforderlich, um Zusammenhänge zu erkennen, die uns heute vielleicht noch gar nicht bewusst sind.
Es liegt auf der Hand, dass die Ergebnisse besser und genauer sind, wenn mehr Daten über einen längeren Zeitraum zur Verfügung stehen. Die Sammlung dieser großen Datenmengen ist derzeit noch einer der Knackpunkte, vor allem aber auch deren Standardisierung. Erst wenn die Daten in einem standardisierten Format vorliegen, können sie mit KI und maschinellem Lernen (ML) ausgewertet werden. Tatsächlich werden also nicht nur Big Data, sondern vielmehr Smart Data benötigt. Typische Daten, die zum Trainieren von ML-Algorithmen verwendet werden könnten, sind:
Strukturelle Daten: Daten, die von Menschen nicht verändert wurden, wie z. B. Röntgenbilder.
Verhaltensbasierte Daten: Standardisierte Daten, die durch menschliches Verhalten beeinflusst werden.
Genetische Daten: DNA- oder RNA-Sequenzen, die aus Blutproben von Patienten extrahiert wurden
Klinisch-chemische Daten: Blutuntersuchungen und die Verwendung anspruchsvollerer und breiterer Ansätze, z. B. Metabolom-Analysen
Aber so einfach ist es dann doch nicht.
Röntgendaten, die durch PET-Scanning von Alzheimer-Patienten oder Patientinnen mit leichten kognitiven Beeinträchtigungen gewonnen werden, sind wertvoll für die Diagnose von Alzheimer, aber das wäre schon zu spät. Es ist sowieso fraglich, ob die Komplexität dieser Methode ein umfassendes Screening älterer Menschen zulassen würde.
Verhaltensdaten, die mit den üblichen mentalen Tests erhoben werden, wären möglicherweise zu schwach und daher ungeeignet für eine verlässliche Standardisierung.
Genetische Daten: Wenn die Patienten keine familiäre Alzheimer-Erkrankung mit bekannten Mutationen haben, sind wir wieder bei der genetischen Veranlagung, die zur einer Krankheit führen kann oder aber auch nicht.
Die bereits erwähnten Biomarker Tau und Beta-Amyloid sind nicht zuverlässig genug, um Alzheimer im vorklinischen Stadium zu diagnostizieren.
Außerdem wissen diejenigen, die sich in der Alzheimer-Forschung arbeiten, dass es eine Fülle von mutmaßlichen Alzheimer-Risikofaktoren gibt. Und keiner von ihnen allein wäre ein zuverlässiger Biomarker oder Indikator für die Diagnose einer präklinischen Alzheimer-Erkrankung.
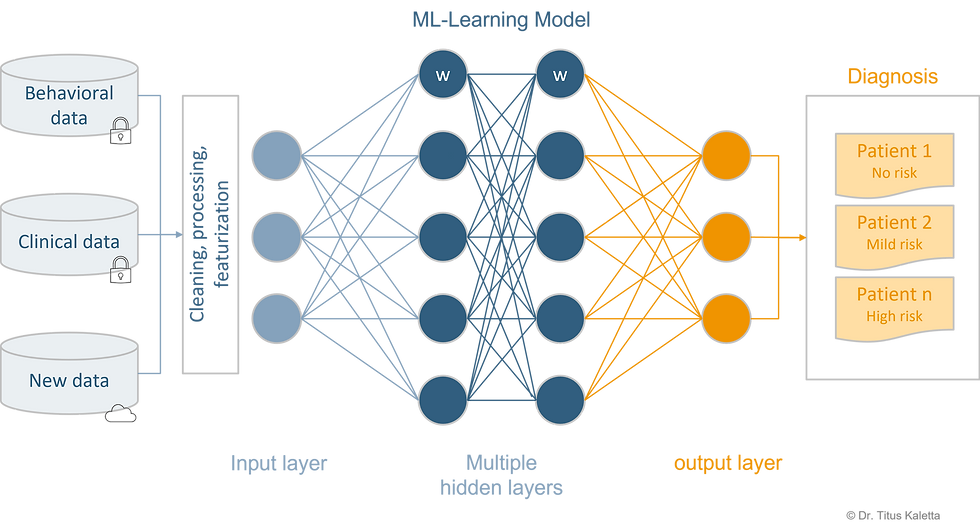
Abbildung 1. Vereinfachtes Modell für maschinelles Lernen: Sammlung von Daten -> Verarbeitung von Daten > Erstellung des ML-Modells -> Einsatz des Modells, das zu einer Diagnose und Risikobewertung führt.
Hier könnte die KI helfen, individuelle Profile für präklinische Alzheimer-Patienten zu erstellen, indem sie eine Kombination von Indikatoren verwendet, die alleine nicht aussagekräftig wären. Anstelle eines oder weniger Marker mit einem definierten Grenzwert für die Diagnose, könnte die KI also verschiedene Risikoprofile mit vielen, auch schwachen Indikatoren für unterschiedliche Patienten erstellen.
Ein vielversprechendes Beispiel ist die Verwendung von Sprach-Signaturen. Das deutsche Start-up, ki-elements, setzt KI zur automatischen Analyse von Sprachmustern ein, die mit früh einsetzender Alzheimer-Erkrankung in Verbindung gebracht werden. Die Daten aus dieser Methode sind hochgradig standardisiert und würden von individuellen Personen stammen. Die israelische Firma Medial EarlySign geht noch einen Schritt weiter: Es entwickelt verschiedene Algorithmen, um subtile, frühe Anzeichen von Krankheiten bei Hochrisikopatienten auf der Grundlage gewöhnlicher elektronischer Gesundheitsakten und vorhandener Laborergebnisse zu erkennen.
Der Einsatz von KI zur Früherkennung von Krankheiten klingt brillant, insbesondere bei sehr frühen und unklaren Anzeichen. Aber wir müssen bedenken, dass auch eine Behandlung, Interception, erforderlich ist, um die Krankheit zu heilen oder zumindest ihren Ausbruch zu verzögern.
Herausforderungen für die Disease Interception
Grundsätzlich kann das Konzept der DI nur funktionieren, wenn:
Die Krankheit bzw. deren Vorstufe vor ihrem Ausbruch mit hoher Sicherheit diagnostiziert wird, um eine Überbehandlung zu vermeiden.
Behandlungsoptionen zur Verfügung stehen, die das Ausbrechen einer solchen Krankheit verhindern können (Änderung des Lebensstils reicht nicht aus) und
Die Bereitschaft des Patienten, mit der Diagnose umzugehen und ein Behandlung zu akzeptieren und zu beginnen.
Ein bekanntes Beispiel ist Angelina Jolie. Bei ihr wurde eine Mutation in einem Brustkrebsgen, BCAR1, festgestellt, das mit einem hohem Brustkrebsrisiko verbunden ist. Sie unterzog sich vorsorglich einer Mastektomie. Diese Entscheidung fiel ihr sicherlich nicht leicht und sie stand vor einem Dilemma: Entweder sie akzeptiert die Mastektomie, obwohl nicht sicher war, dass sie Brustkrebs entwickeln würde, oder sie lehnt die Operation ab, mit dem Risiko, dass sich der Krebs schnell unentdeckt entwickeln würde und die Behandlung dann sehr schwierig wäre. DI hätte eine Lösung sein können, um den Ausbruch von Brustkrebs früh genug für eine sofortige und wirksame Behandlung zu erkennen, aber auch, um eine Behandlung zu vermeiden, wenn sich der Krebs gar nicht entwickelt.
Bleiben wir bei unserem Beispiel Alzheimer. Für Alzheimer gibt es heute keine Heilung. Es ist daher eine ethische Frage, das Auftreten einer Krankheit vorherzusagen, dem Patienten aber sagen zu müssen, dass sie oder er nichts dagegen tun kann. Das Konzept DI kann nur dann erfolgreich sein, wenn es wirklich möglich ist, den Ausbruch der Krankheit zu verhindern. Ein weiterer Punkt, den es zu berücksichtigen gilt, ist, dass die Nebenwirkungen der Behandlung sehr gering sein müssen oder die Dauer der Behandlung so kurz sein muss, dass keine nennenswerten Nebenwirkungen auftreten. So gibt es beispielsweise eine Debatte über den richtigen Beginn des Einsatzes von Statinen zur Vorbeugung koronarer Herzkrankheiten, da nicht alle Patienten Statine gut vertragen. Eine weitere Herausforderung besteht darin, geeignete klinische Studien zu konzipieren. Die Durchführung einer klinischen Studie mit klinisch gesunden Patienten unter Verwendung eines neuen Arzneimittels wird ethische Fragen aufwerfen.
Perspektive für die Disease Interception
Disease Interception ist ein vielversprechender Ansatz, der erhebliche Auswirkungen auf die Behandlung von Alzheimer und anderen chronisch-progredienten Krankheiten haben könnte. Man darf jedoch nicht vergessen, dass es sich hierbei um ein noch junges Forschungsgebiet handelt und dass die Strategie der DI einige Einschränkungen aufweist. Der Einsatz von KI kann dazu beitragen, Korrelationen zu finden, die von Menschen sonst nur schwer zu erkennen wären. Außerdem könnten schwache oder indirekte Indikatoren kombiniert werden, um patientenspezifische Risikoprofile zu erstellen. Die Hoffnung allerdings, den Schalter, der die Entwicklung einer Krankheit einleitet, zu finden und rechtzeitige Maßnahmen einzuleiten, mag noch Science-Fiction sein, aber mit jedem Monat und Jahr mit dem eine Behandlung früher beginnt, erhöht sich die Wahrscheinlichkeit, dass die Krankheit gestoppt oder zumindest verzögert wird.
Photo by shutterstock.



Kommentare